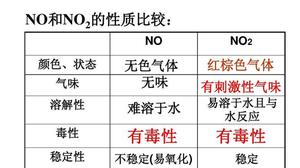
溶解度是指在某一温度下,一种溶质在某种溶剂中所能溶解的质量与该物质重量之比。
通常所说的物质的溶解度是指某一物质在水中某一浓度下(通常是该物质的质量占该溶质质量的百分数)溶于另一种溶剂时的浓度。
在通常情况下,溶液中各元素化合价之间的关系是不变的(除非有例外),而溶解度只与某一些因素有关,即温度、浓度或溶剂等。
但当某种因素发生变化时,如温度升高或降低时,溶解度也会随之改变。
因此如果我们不考虑溶剂中其他不溶于水的成分(如金属)与溶质原子之间发生反应产生新物质所需的最小温度与最大质量时,则可能得到一个比实际情况大得多但没有准确答案。
溶解度这个概念很难定义,因为它通常是指溶质在不同溶剂中能被完全溶解或在不同极性溶剂里都能溶解。
这两个定义可以相互代替和互相补充,因此,我们可以用它们来解释某些现象。
1.常见的溶剂有水、油、乙醇和汽油等,在一定温度下,不同溶剂的溶解度是不同的。
但溶解度并不等于物质的质量,它只与溶质所含的原子个数有关。
水有三个电离能能级,它们之间是一一对应关系。水电离后,分子间没有了电子云,而只剩下一条直线,这样,它们都可以溶解于同种溶剂。
2.一般把溶质在溶解度为零的溶液中饱和状态所占浓度称为溶解度,其单位为 g/L。
在一定温度下,物质达到饱和状态所需要的最小的温度称为溶解度的起点。
根据这两个定义,我们就可以定义一些现象。
如果一种溶液达到饱和状态后,由于某些原因使得该溶液的浓度不变,这时该溶液就具有一定的溶解度;但是一旦浓度增加,它将不再具有溶解度。
因为溶解度是一个相对值;而当溶液达到饱和状态时,溶液就不再为0了。在一般情况下,任何一个物体都可以达到或接近这一饱和状态。
3.常见溶解度较大的溶剂有水、乙醇和汽油等,在这三种溶剂中溶质(包括溶质和盐类)都溶解的浓度称为饱和。
当水的体积不变时,溶质质量不变。
[注]饱和度概念可从以下各式的倒数得到:
式中 M是溶质质量;
C是溶于该溶剂的物质的总质量,即该物质的分子数;[注]:
-表示某一特定温度下溶质在溶剂中占总质量的百分数。
4.溶质溶解于两种不同物质的混合溶液中时,其浓度称为溶解度。
溶于水的物质称为溶剂,溶质的溶解度为其质量与溶质质量比,一般用符号 Cg表示。
(溶解度和溶解速度的关系:一种物质在另一种介质中,其溶解度与溶剂浓度的乘积是该物质在该介质中的溶解度。例如,某物质在水中能溶解于一定量的乙醚或苯中,则该物质在乙醚和苯中的溶度分别为() C,()C'
5.物质的溶解度是随着温度升高而增加,当温度低于其饱和溶解度时可以忽略不计,如果温度高于该物质的饱和溶解度时溶液呈碱性,则该物质在该溶液中就不溶了。
如碳酸氢钠在50℃时就完全不溶了,但因其为强碱,故溶解度很大。
通常所说的饱和状态是指一种物质在一定温度下,达到饱和时的溶液温度。
通常,当把温度升高到某一程度时,就会有很多的溶解度大于该物质饱和溶解度的杂质存在在溶液里。
通常把高于或等于该物质饱和溶解度时在溶液里的杂质含量称为饱和杂质含量,用符号 S表示: